| 중국, ′23년 상반기 20종의Ⅰ급 신약과 25개의 Ⅲ급 의료기기 출시 | ||
|
||
|
□ 재발성 골수암 등 생물학적 제제와 자기공명 레이저장치 등 의료기기 출시 (7.17)
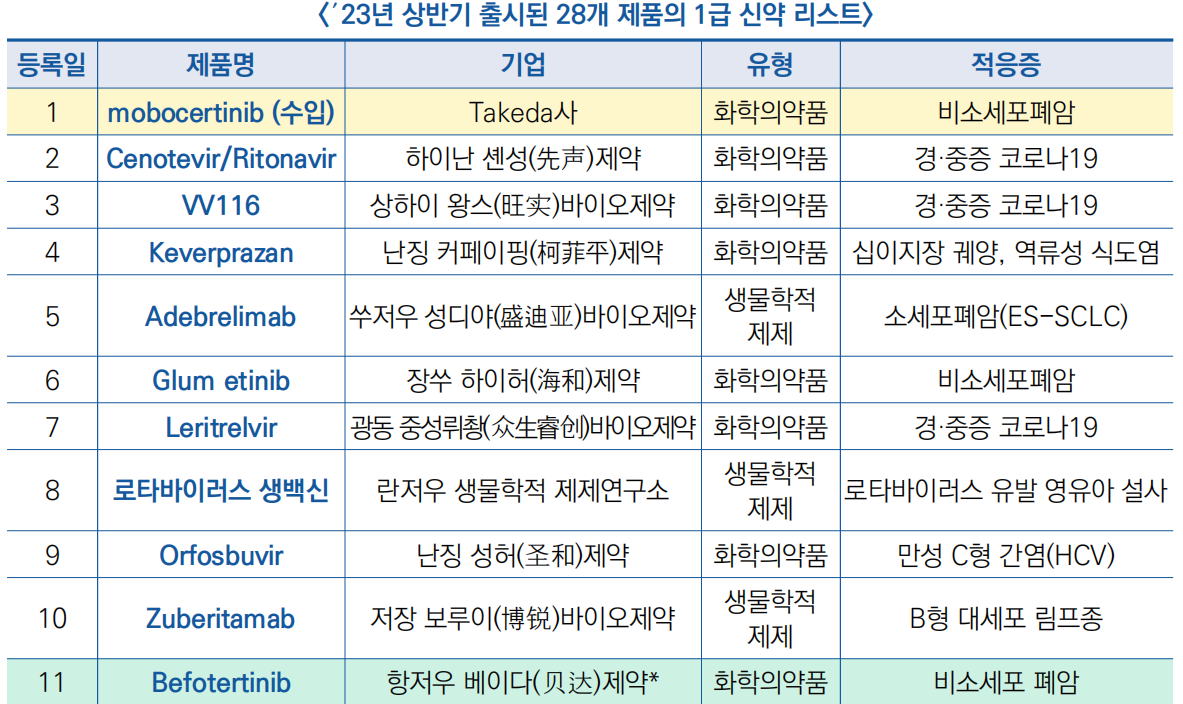
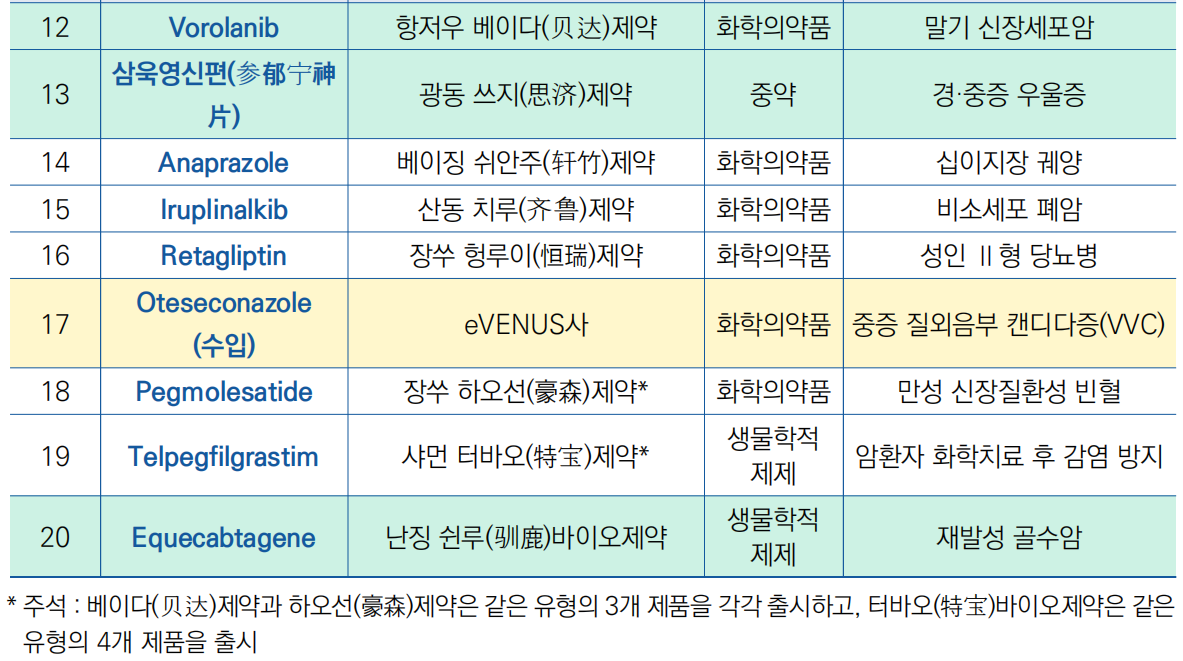
○ ′23년 7월 기준, 국가약품감독관리국(NMPA)은 총 28개 제품(20종)의 Ⅰ급 혁신 의약품 시판을 승인
- 동 시기 FDA가 새로 승인한 분자신약은 18종과 생물학적 제제(BLA) 10종을 포함해 총 63종의 신약(NDA/BLA)를 승인했으며, EU의 EMA는 총 25종의 신약을 승인
- 중국은 화학의약품 19개 제품(14종), 생물학적 제제 8개 제품(5종) 및 중약 신약 1개를 포함하여 총 28개 제품(20종)의 혁신 의약품 의약품을 출시
- 총 19개 기업이 해당되며, 그 중 베이다(贝达)제약은 2종의 화학의약품을 승인, 쉰루(驯鹿)제약 등 5개 기업은 생물학적 제제를 승인, 쓰지(思济)제약이 유일한 중약 신약을 승인받음
- 그 외 미국의 Takeda, eVENUS 등 해외 기업이 중국시장에서 2종의 화학의약품이 승인됨
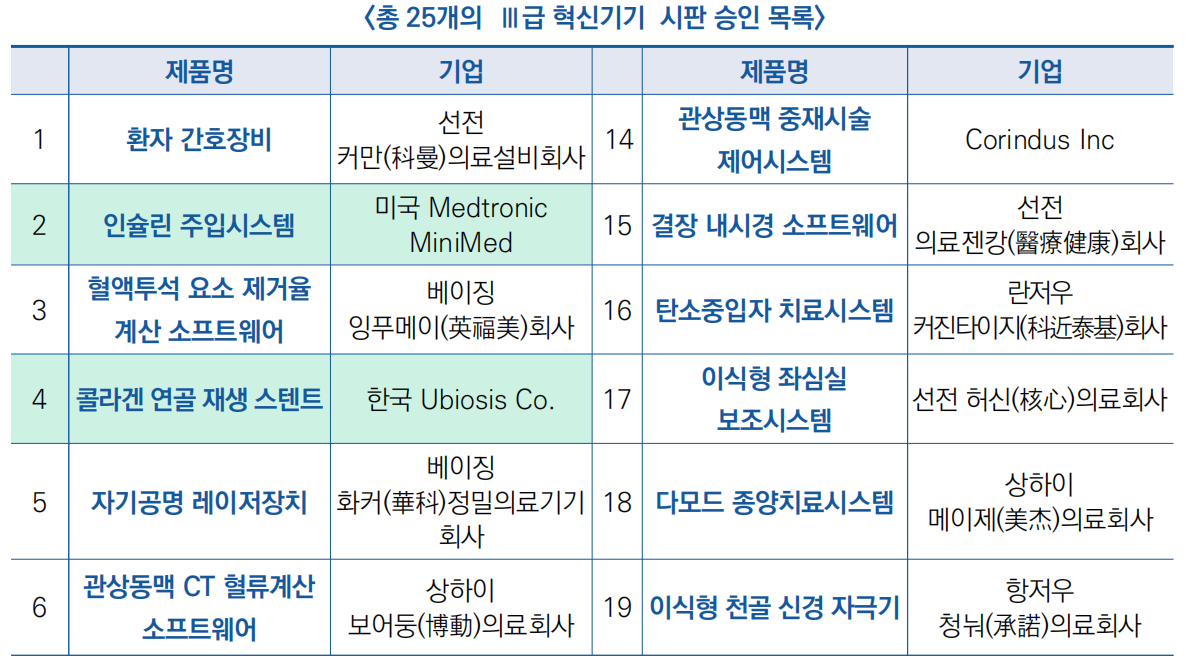
  ○ ′23년 상반기, 국가약품감독관리국(NMPA)은 글로벌 의료기기 분야에서 총 25개의 Ⅲ급 혁신 장치의 시판을 승인
- 동시기 FDA는 총 1,575개의 제품을 승인했으며, 정형외과기기, 일반기기, 성형외과기기, 방사선장치, 심혈관 장치 및 종합병원 등이 승인
- 총 25개 승인된 의료기기 중 미국, 한국, 캐나다 등 해외 의료기기업은 인슐린 주입시스템, 콜라겐 연골 재생 스텐트, 인공수정체, 혈관내 영상설비 등 기기를 출시
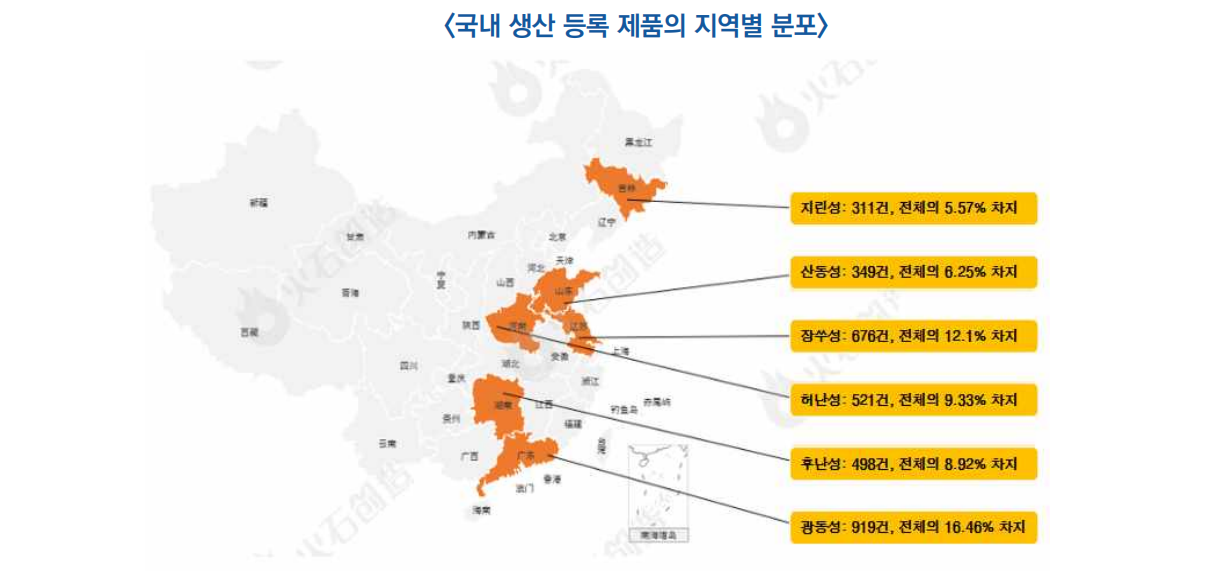
  ○ 지역적 분포를 보면, 국내 생산 등록 제품(Ⅰ,Ⅱ,Ⅲ급)에 대한 가장 많은 승인은 광동성(919건), 장쑤성(676건), 허난성(521건)으로 나타남
 <참고자료>
2023上半年药械创新成果报告:国内20款创新药获批上市
|
- 정책동향
- 이슈리포트
- 통계DB
- 통계DB
