| 허페이물질과학 연합팀, 농도에 의존하는 자발적 세포사멸 | ||
|
||
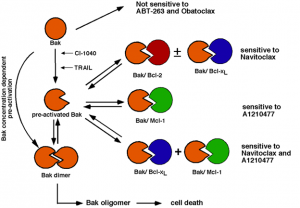 최근, 중국과학원 헤페이(合肥)물질과학연구원 의학물리·기술센터 분자병리연구실 연구원 다이하이밍(戴海明)은 미국메이오(Mayo)의학대학, 미국존스홉킨스(Johns Hopkins)의학대학의 연구원들과 공동으로 세포 사멸에 관한 연구에서 새로운 성과를 확보하였다. 해당 연구 성과는 2015년 10월에 출간한 Genes and Development 잡지에 Constitutive Bak activation as a determinant of drug sensitivity in malignant lymphohematopoietic cells라는 제목으로 게재되었다. 세포 사멸은 유전자가 제어하는 자발적인 세포 생리성 자살 현상으로서 다세포생물의 발육, 면역 및 생식계통 성숙 등 생리 과정에서 중요한 작용을 일으킬 뿐만 아니라 종양의 발생 및 치료 과정에서도 중요한 작용을 일으킨다. 세포 사멸의 주요 신호 전달 경로에는 사멸 수용체가 유도하는 세포 사멸 경로와 미토콘드리아가 유도하는 세포 사멸 경로 등 2가지가 있다. 미토콘드리아가 유도하는 세포 사멸 경로는 Bcl-2 단백질 패밀리의 제어를 받는다. Bcl-2 단백질 패밀리의 구성원인 Bak는 활성화된 후 직접 미토콘드리아 외막을 투과하는 기능을 갖고 있다. 미토콘드리아 외막이 천공(perforation)된 후 미토콘드리아 내막과 외막 사이의 시토크롬 C. Smac 등과 같은 단백질 분자들이 방출되어 하위의 세포 사멸 신호인 카스파제(Caspase)를 활성화시킨다. 연구팀은 최초로 Bak가 오직 BH3 도메인을 함유한 단백질(BH3-only protein)에 의하여 활성화될 수 있을 뿐만 아니라 또한 세포내에서 농도 의존의 자발적인 활성화 과정이 발생한다는 것을 발견하였다. 이 현상을 Bak 구성성(constitutive) 활성화라고 칭하였다. 혈액 종양 세포에서 해당 구성성 활성화는 최대로 80%에 달하며, 또한 Bak의 구성성 활성화 방식은 종양 세포가 약물에 대한 민감성과 관련이 있음을 보여주고 있다. 연구 과정에서 또한 급성 골수세포성 백혈병 환자에게서 발생하는 Bak 저발현은 종양의 약물 내성 및 재발과 관련성이 있다는 것을 발견하였다. 해당 연구 결과는 Bak의 활성화 과정을 연구하는데 새로운 메커니즘을 제공할 수 있을 뿐만 아니라 또한 항종양 약물의 치료 효과를 예측하는데 새로운 아이디어를 제공할 것으로 전망된다. 정보출처 : http://www.cas.cn/syky/201511/t20151118_4466326.shtml |
- 정책동향
- 이슈리포트
- 통계DB
- 통계DB
